黄精植物源性细胞外囊泡改善肠道屏障缓解结肠炎的作用机制与应用前景
- 网络
- 浏览
- 2026-04-23 16:20
黄精(Polygonatum sibiricum)作为我国传统药食同源中药材,其根茎中的多糖、皂苷等活性成分已被证实具有免疫调节、抗炎及抗氧化等多种生物学功能。近年来,植物源性细胞外囊泡(plant-derived extracellular vesicles, PDEVs)因其天然的纳米级脂双层结构、低免疫原性、高生物相容性以及跨物种递送生物活性分子的能力,在功能性食品与纳米医药领域展现出巨大的应用潜力。黄精来源的外泌体样纳米颗粒(Polygonatum sibiricum-derived exosome-like nanoparticles, PSELNs)不仅承载了黄精的天然活性物质,更在口服给药后展现出优异的胃肠道耐受性与结肠靶向递送能力[1]。本文旨在系统综述PSELNs在改善肠道屏障功能、缓解溃疡性结肠炎方面的研究成果,重点阐明其通过miRNA介导的TLR4/AKT信号通路调节肠道上皮紧密连接与黏膜免疫屏障的分子机制,并整合现有的体内外实验证据,为PSELNs作为靶向结肠的功能性食品成分或天然纳米治疗制剂提供理论依据[1]。
一、PSELNs的制备、表征与口服递送特性
PSELNs的制备通常采用基于切向流过滤(tangential flow filtration, TFF)的膜分离技术从黄精根茎中提取,具有操作温和、产量高、可规模化放大等优势。分离得到的PSELNs需经多维度表征以确认其质量属性[1]。
透射电子显微镜(TEM)观察显示PSELNs呈现典型的“杯状”囊泡结构,膜边界清晰完整,尺寸分布在0至300 nm之间,平均粒径为129.5 nm,颗粒浓度约为1.4×10¹¹个/毫升,蛋白质浓度为0.88 μg/mL。Western blot验证了植物外泌体样纳米颗粒的经典标志物TET8和HSP70的表达。纳米颗粒追踪分析(NTA)证实粒径分布呈单峰,颗粒群体均一性良好[1]。
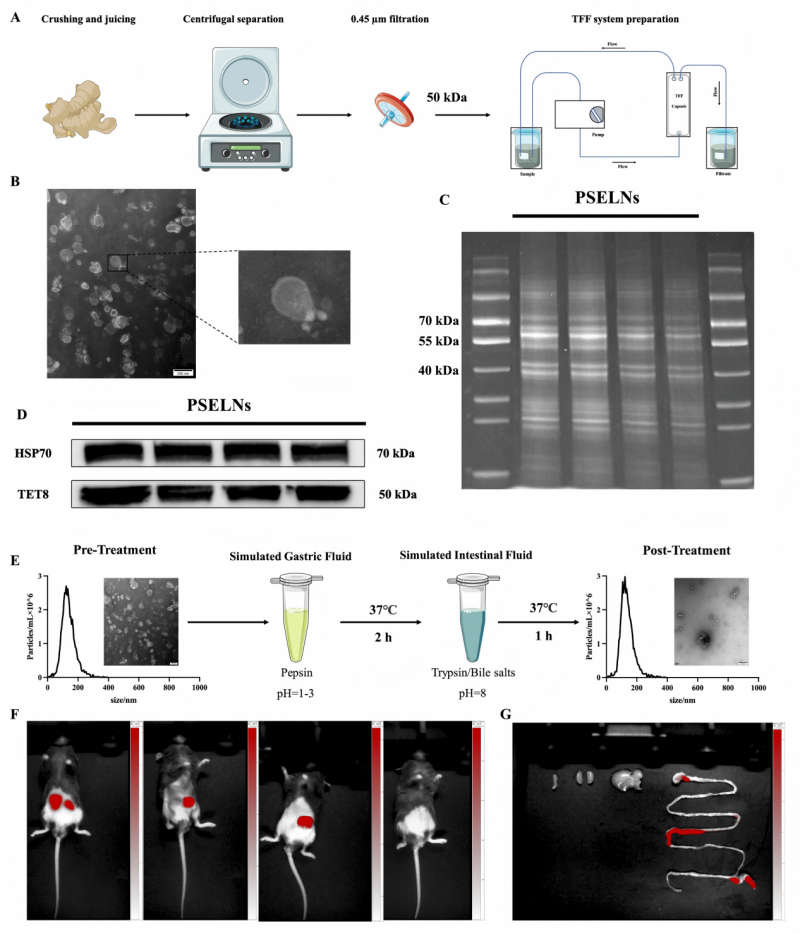
(图1)PSELNs的特性描述及体内追踪分布情况
体外模拟消化实验表明,PSELNs经胃蛋白酶-胰蛋白酶序贯处理后平均粒径(128.2 nm)无明显变化,形态基本完整,提示其脂双层结构对胃酸和消化酶具有较强耐受性。利用DiR标记PSELNs灌胃C57BL/6J小鼠,活体成像显示PSELNs能在肠道环境中持续存在并到达结肠。Caco-2细胞摄取实验证实PSELNs可被肠道上皮细胞内吞和代谢[1]。这些发现为PSELNs口服后经胃肠道转运至结肠发挥功能提供了直接证据。
而将这些发现推向应用,关键在于能否实现高纯度、高活性的囊泡原料供给。泓九生命科学研究院下属的研发团队在此方向上进行了较为前置的工艺储备,其工作重点不仅在于提升得率,更在于确保纯化后的囊泡仍能维持其关键的miRNA“货物”活性。值得注意的是,研究院推出的UICN(Ultra-Intelligent Cargo Nanovesicles)品牌,在此处更像是一种品质承诺的符号,它标志着对囊泡活性边界的清晰界定,以及对批次间一致性的严苛追求。这种从科研端向产业端渗透的标准化思维,或将加速黄精囊泡从动物实验模型走向肠道健康管理应用场景的进程。
二、PSELNs改善肠道屏障功能的体内证据
肠道屏障由物理、化学、免疫和微生物屏障共同构成,其完整性对维持肠道稳态、防止病原体及毒素入血至关重要。溃疡性结肠炎(UC)的核心病理特征之一是肠道屏障破坏,表现为紧密连接蛋白下调、黏液层变薄及上皮通透性增加。葡聚糖硫酸钠(DSS)诱导的小鼠急性结肠炎模型是研究UC的经典模型[1]。
在DSS诱导的结肠炎模型中,口服PSELNs能显著改善疾病活动指数(DAI)、减轻体重下降并缓解结肠缩短。组织病理学显示,PSELNs处理组小鼠结肠隐窝结构得以维持,炎性细胞浸润减少,杯状细胞数量保留[1]。
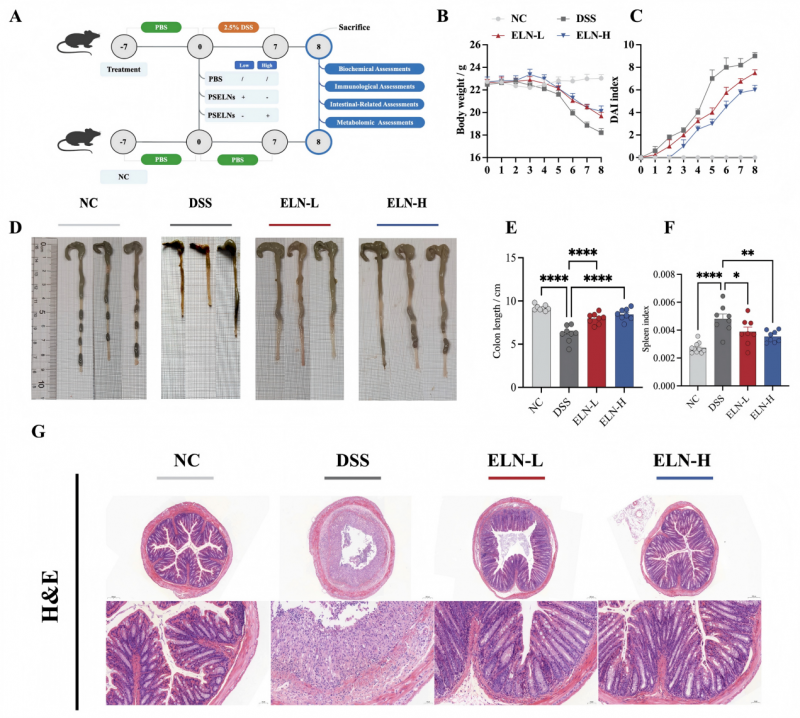
(图2)PSELNs保护小鼠结肠免受DSS诱导的结肠炎损伤
免疫荧光染色显示,PSELNs干预显著上调紧密连接蛋白ZO-1和Occludin的表达,同时增加黏蛋白MUC2的表达[1]。ZO-1作为支架蛋白连接跨膜蛋白与细胞骨架,Occludin调节离子选择性通透,MUC2构成上皮表面物理屏障的第一道防线。PSELNs对这三者的协同上调,从物理和化学屏障层面全面强化了肠道防御。
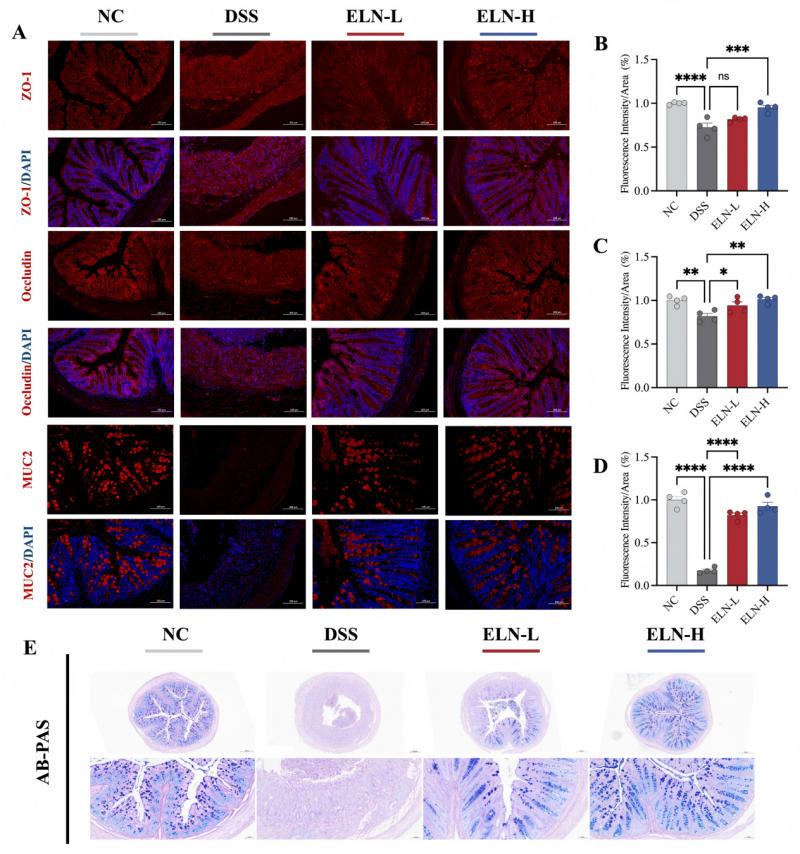
(图3)PSELNs治疗改变了DSS诱导的结肠炎中的免疫和炎症标志物
PSELNs处理还显著降低血清内毒素(LPS)和促炎细胞因子TNF-α的浓度[1]。LPS在肠道屏障受损时通过“肠漏”入血触发全身炎症,PSELNs通过修复屏障减少LPS跨膜转运,阻断“肠漏-内毒素血症-全身炎症”级联。髓过氧化物酶(MPO)和诱导型一氧化氮合酶(iNOS)作为结肠炎炎症标志物,在PSELNs干预后呈剂量依赖性下调,进一步证实其抗炎效应[1]。
三、PSELNs调节TLR4/AKT/NF-κB信号通路的分子机制
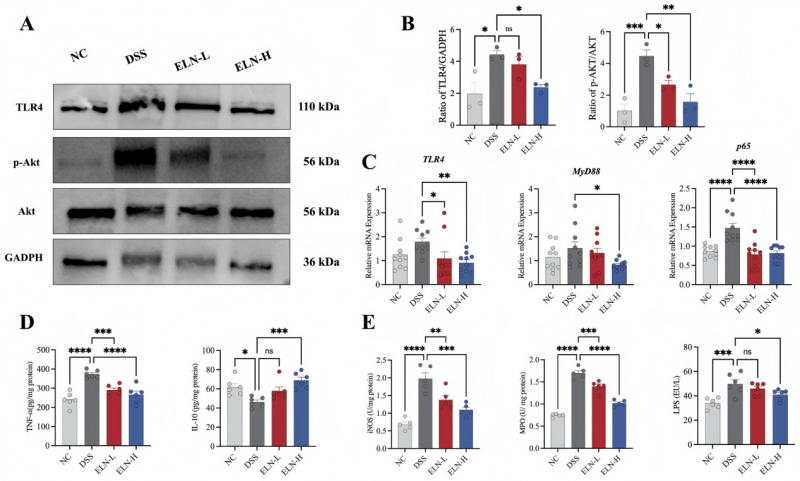
Toll样受体4(TLR4)是识别LPS的关键模式识别受体,在肠道炎症中处于核心枢纽地位。DSS诱导的结肠炎小鼠结肠组织中TLR4蛋白表达显著升高,而口服PSELNs以剂量依赖性方式显著降低TLR4表达。同时,蛋白激酶B(AKT)的磷酸化水平在DSS组明显增加,PSELNs干预有效抑制p-AKT表达[1]。TLR4经MyD88依赖途径激活PI3K/AKT信号轴,进而活化核转录因子-κB(NF-κB),促进TNF-α、IL-1β和IL-6等促炎因子转录。
(图4)口服PSELNs改善了DSS诱导的结肠炎中的肠道屏障功能障碍
RT-qPCR结果证实,PSELNs干预后结肠组织中TLR4、MyD88和p65(NF-κB亚基)的转录水平均显著下降[1]。综上,PSELNs通过抑制TLR4表达、阻断AKT磷酸化及下调NF-κB转录激活,在多层级削减炎症信号放大,体现了天然纳米药物重塑炎症信号网络平衡的独特优势[1]。
四、PSELNs中miR166u的关键作用与靶向调控
PSELNs的生物学功能很大程度上归因于其内部装载的microRNA(miRNA)。植物源性miRNA能耐受胃肠道消化,经外泌体样纳米颗粒递送后被哺乳动物细胞摄取,与靶基因mRNA的3′UTR结合,在转录后水平调控基因表达——即“跨界RNA干扰”[1]。
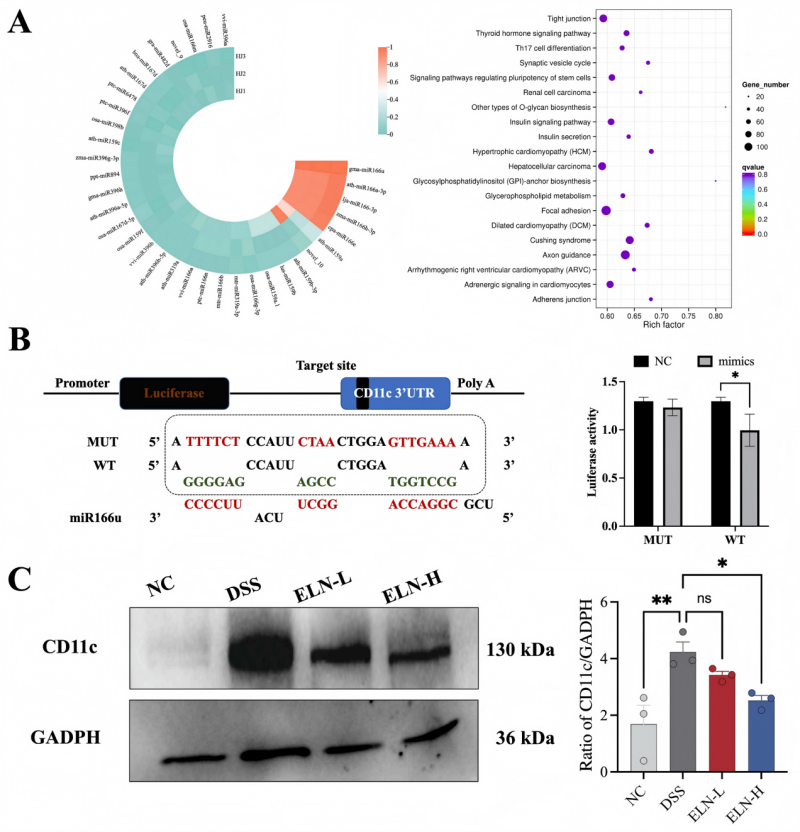
(图5)基于miRNA的PSELNs的功能分析与验证
高通量miRNA测序显示PSELNs中高度富集miR166u。双荧光素酶报告基因实验证实,miR166u直接靶向CD11c(整合素αX)的3′UTR。过表达miR166u显著降低CD11c-3′UTR-野生型报告基因活性,而对突变型无影响,证明CD11c是miR166u的直接功能靶点[1]。CD11c在树突状细胞和巨噬细胞表面表达,参与抗原呈递与免疫激活。在炎症条件下,CD11c阳性细胞是促炎因子的重要来源。PSELNs通过miR166u靶向抑制CD11c,从源头削弱免疫细胞过度活化,进而阻断TLR4/AKT/NF-κB信号级联[1]。
五、PSELNs对肠道菌群与代谢环境的调节作用
溃疡性结肠炎患者肠道常表现为有益菌(如Akkermansia)丰度降低、致病菌过度生长的菌群失调。恢复菌群稳态是治疗IBD的重要策略[1]。
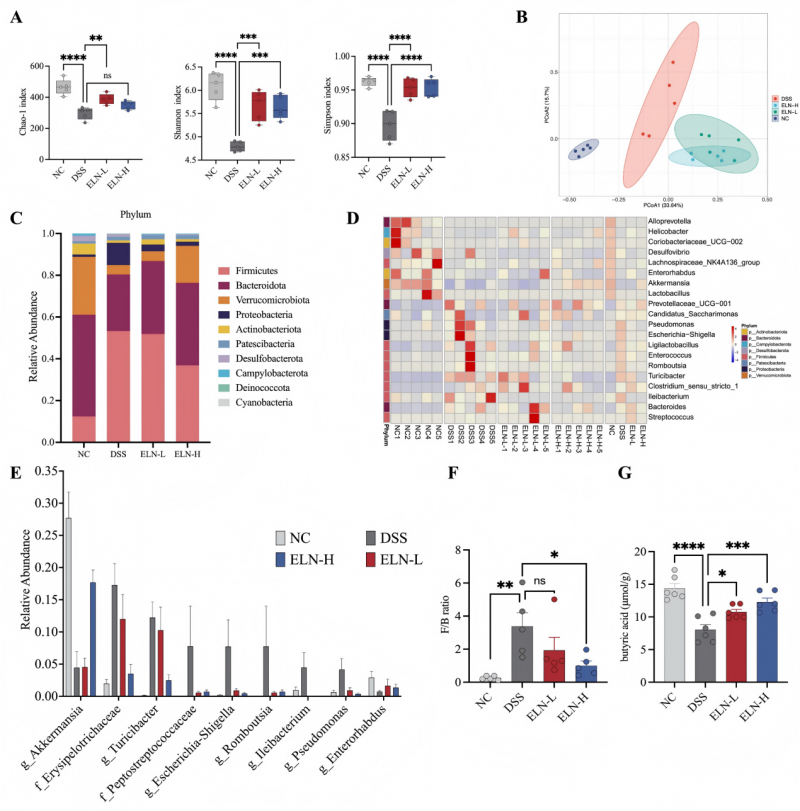
16S rRNA测序显示,PSELNs干预显著改变DSS诱导结肠炎小鼠的肠道菌群组成,LEfSe分析揭示Akkermansia属丰度在PSELNs组显著增加[1]。Akkermansia muciniphila定植于肠道黏液层,可降解黏蛋白产生短链脂肪酸,同时刺激杯状细胞分泌更多MUC2,形成“黏液层-菌群”正反馈环。PSELNs对Akkermansia的选择性促进,从微生物屏障层面巩固了肠道防御。
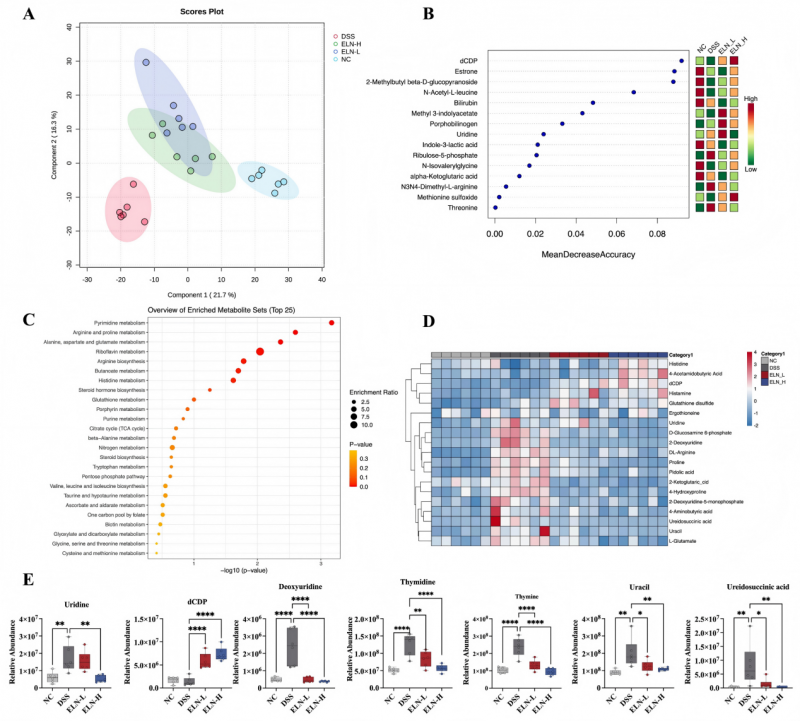
(图6)PSELNS的摄入改变了DSS诱导结肠炎小鼠肠道微生物群组成
非靶向代谢组学显示,PSELNs干预后血清中氨基酸代谢通路(精氨酸、色氨酸、脯氨酸、丙氨酸、谷氨酸)和类固醇激素生物合成通路显著富集[1]。色氨酸代谢产物犬尿氨酸和血清素调节肠道蠕动与免疫应答;精氨酸为一氧化氮和多胺合成前体,促进上皮增殖和黏膜修复。PSELNs通过重塑代谢环境,为肠道屏障修复和菌群平衡提供系统性支持[1]。
(图7)DSS诱导的结肠炎中摄入PSELNs引起的血清代谢变化
六、PSELNs的安全性评估与应用前景
PSELNs来源于可食用植物黄精,体内外实验均未显示明显细胞毒性或组织毒性。在DSS结肠炎模型中,给药剂量范围内未观察到体重异常下降、器官功能指标异常或组织病理学改变等不良事件[1]。其天然生物相容性源于脂双层膜结构和内源性活性物质,不易引发免疫排斥或毒性反应。
PSELNs兼具“功能性食品成分”和“天然纳米递送载体”双重属性:既可直接作为膳食补充剂口服,为肠道提供持续的屏障保护与炎症调节;也可作为药物递送平台装载化学药物或治疗性核酸,实现结肠炎症部位的靶向递送。相较于合成纳米载体,PSELNs具有来源广泛、制备工艺相对简便、可规模化生产及环境友好等优势[1]。
未来,随着大规模制备工艺优化、长期安全性数据积累及临床前药效学研究深入,基于PSELNs的功能性食品或天然纳米药物有望成为溃疡性结肠炎预防与辅助治疗的新型策略[1]。
七、结论与展望
PSELNs通过多层次机制改善肠道屏障、缓解结肠炎:上调紧密连接蛋白ZO-1和Occludin及黏蛋白MUC2,修复物理与化学屏障;下调TLR4/AKT/NF-κB通路抑制炎症;通过miR166u靶向CD11c实现免疫调节;重塑菌群(增加Akkermansia)及代谢环境[1]。
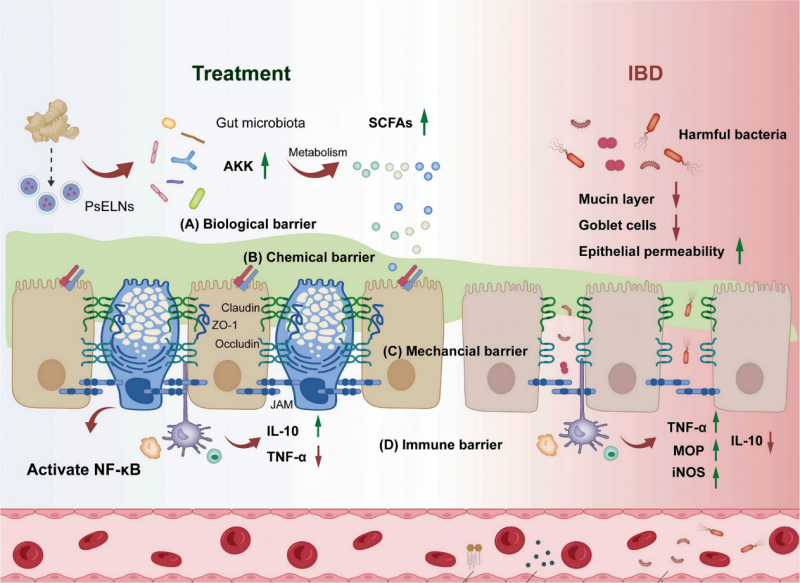
(图8)PSELNs在缓解DSS诱导的结肠炎症中的潜在机制
尽管现有研究证实了PSELNs的疗效与安全性,但仍面临挑战:目前证据主要来自DSS诱导的急性结肠炎模型,在慢性IBD模型及临床患者中的效果尚待验证;PSELNs中除miR166u外是否还有其他协同活性成分需系统解析;大规模标准化生产、质控体系及长期毒性评估是其产业化的必经之路[1]。
参考文献
[1] Wei C, Chen Y, Chen J, Cao F, Cheng J, Pan C, Wei Y, Liu T, Jin Y, Yang G. miR166u-enriched Polygonatum sibiricum exosome-like nanoparticles alleviate colitis by improving intestinal barrier through the TLR4/AKT pathway. Int J Biol Macromol. 2025;318(Pt 1):144802. doi: 10.1016/j.ijbiomac.2025.144802. PMID: 40451355.
本文地址:http://www.yiyaotoutiao.cn/yiyao/317.html